ศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์โรงพยาบาลรามาธิบดี มหาวิทยาลัยมหิดล อัพเดตสถานการณ์โรคโควิด-19 และสายพันธุ์ที่กำลังระบาด ว่า ในประเทศไทยพบ "กลุ่ม XBB" ประมาณร้อยละ 52 และ "XBB.1.16" ร้อยละ 9.4 ยังต้องจับตาแอนติบอดีสำเร็จรูป "หนึ่งเดียว" ที่สามารถทำลายโอไมครอนสายพันธุ์ย่อย XBB.1, XBB.1.5, และ XBB.1.16
ล่าสุดองค์การอนามัยโลกประกาศอัปเกรดให้ XBB.1.16 จาก "สายพันธุ์ภายใต้การตรวจสอบ" เป็น "สายพันธุ์ที่น่าสนใจ" แต่ยังไม่ถึงขั้น "สายพันธุ์ที่น่ากังวล" เนื่องจากพบผู้ติดเชื้อเพิ่มขึ้นอย่างต่อเนื่อง และมีข้อได้เปรียบในการเติบโต-แพร่ระบาด (relative growth advantage) เหนือกว่าสายพันธุ์อื่น
กลุ่มนักวิจัยสหรัฐวิเคราะห์ข้อมูลจากผู้ติดเชื้อโควิด-19 และข้อมูลการกลายพันธุ์ของไวรัสแต่ละสายพันธุ์ด้วยโปรแกรมคอมพิวเตอร์สมรรถนะสูง สรุปว่า การฉีดวัคซีนเพียงอย่างเดียวยังไม่เพียงพอ ควรผนวกกับมาตรการอื่น เช่น กินร้อน, ช้อนกลาง, ใส่หน้ากาก, เว้นระยะห่าง, ใช้ยาต้านไวรัส, และใช้แอนติบอดี ฯลฯ เพื่อช่วยลดการกลายพันธุ์และควบคุมการระบาดโควิด-19 อย่างมีประสิทธิภาพ
ส่วนที่ผู้เชี่ยวชาญบางคน เรียกโอไมครอน XBB.1.16 ว่า อาร์คทูรัส (Arcturus) ตามชื่อดาวที่สว่างที่สุดในซีกโลกเหนือ แต่องค์การอนามัยโลกจะไม่ตั้งชื่อให้ เพราะมีข้อกำหนดว่า จะกำหนดชื่อภาษากรีกให้เฉพาะโควิดสายพันธุ์ที่น่ากังวล (VOC: variant of concern) เท่านั้น
การตรวจคัดกรองกลุ่มโอไมครอนลูกผสม XBB รวมถึง XBB.1.16
ปลายเดือนมีนาคม พ.ศ. 2566 พบการระบาดของโอไมครอนลูกผสม XBB.1.16 ในหลายประเทศ และ 1 เมษายน 2566 ศูนย์จีโนมฯ ร.พ. รามาธิบดี รายงานพบผู้ติดเชื้อ XBB.1.16 รายแรกในประเทศไทยอาศัยข้อมูลรหัสพันธุกรรมจากฐานข้อมูลโควิดโลก "จีเสส (GISAID)"
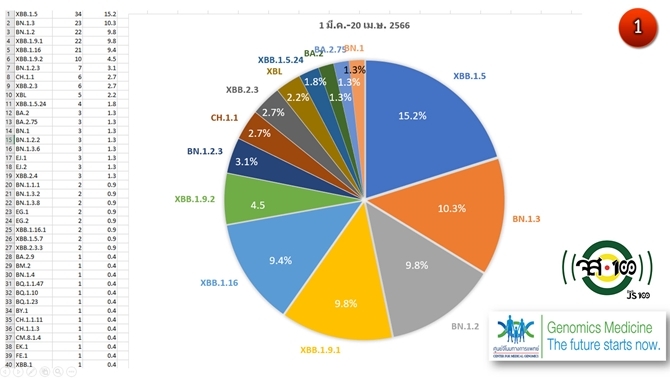
วันที่ 21 เมษายน 2566 ผลการดึงข้อมูลรหัสพันธุกรรมจากฐานข้อมูลจีเสส พบโอไมครอน 14 สายพันธุ์ย่อยที่พบมากในประเทศไทยเรียงตามลำดับ ดังนี้ โดยพบกลุ่มไวรัสสายพันธุ์ XBB* ประมาณร้อยละ 52 และ XBB.1.16 อยู่ในลำดับที่ 5 จำนวน 21 รายจาก 224 ราย หรือคิดเป็นร้อยละ 9.4 จากเชื้อโควิด-19ทั้งหมดที่ถอดรหัสพันธุกรรมภายในประเทศในช่วง 1 เดือนครึ่งที่ผ่านมา
XBB.1.5 จำนวน 34 ราย (15.2%)
BN.1.3 จำนวน 23 ราย (10.3%)
BN.1.2 จำนวน 22 ราย (9.8%)
XBB.1.9.1 จำนวน 22 ราย (9.8%)
XBB.1.16 จำนวน 21 ราย (9.4%)ลำดับที่ 5
XBB.1.9.2 จำนวน 10 ราย (4.5%)
BN.1.2.3 จำนวน 7 ราย (3.1%)
CH.1.1 จำนวน 6 ราย (2.7%)
XBB.2.3 จำนวน 6 ราย (2.7%)
XBL จำนวน 5 ราย (2.2%)
XBB.1.5.24 จำนวน 4 ราย (1.8%)
BA.2 จำนวน 3 ราย (1.3%)
BA.2.75 จำนวน 3 ราย (1.3%)
BN.1 จำนวน 3 ราย (1.3%)
ศูนย์จีโนมฯ รพ. รามาธิบดี ได้พัฒนาชุดตรวจเชื้อโอไมครอนของกลุ่มสายพันธุ์ย่อย XBB* เพื่อให้สามารถแยกจากสายพันธุ์อื่นเสร็จเป็นที่เรียบร้อยด้วยเทคโนโลยี Mass array genotyping โดยตรวจรู้ผลภายใน 24-48 ชั่วโมง ซึ่งมีค่าใช้จ่ายสูงกว่าการตรวจ PCR (ที่ไม่อาจตรวจทราบสายพันธุ์) เพียงเล็กน้อย และประหยัดกว่าการถอดรหัสพันธุกรรมไวรัสทั้งจีโนม เนื่องจากมีความจำเป็นสำหรับแพทย์เพื่อเลือกใช้ยาต้านไวรัสประเภทแอนติบอดีสำเร็จรูปกับผู้ป่วยได้ถูกต้องและทันท่วงที ซึ่งทีมนักวิจัยประเทศญี่ปุ่นนำโดย ดร. เคอิ ซาโต้ (Kei Sato) จากมหาวิทยาลัยโตเกียว พบว่ามีแอนติบอดีสำเร็จรูปเพียงชนิดเดียวคือ "โซโทรวิแมบ (Stromab)" ที่แสดงฤทธิ์ต้านไวรัสโอมิครอนสายพันธุ์ย่อย XBB.1, XBB.1.5, XBB.1.16 ได้ดี ส่วนแอนติบอดีสำเร็จรูปประเภทอื่นไม่สามารถเข้าจับและทำลายบรรดาโอไมครอนสายพันธุ์ย่อย XBB* เนื่องจากมีการกลายพันธุ์ไปมากจนแอนติบอดีจำไม่ได้
ศูนย์จีโนมฯ รพ. รามาธิบดี ยังเร่งพัฒนาต่อยอดชุดตรวจในปัจจุบันให้สามารถแยกโอไมครอนสายพันธุ์ย่อย ครอบคลุมสายพันธุ์ที่กำลังเป็นปัญหา อาทิ XBB.1.16,XBB.1.9.1, และ XBB.1.5 ออกจากสายพันธุ์อื่นเพื่อการรักษาแบบมุ่งเป้าหรืออย่างจำเพาะด้วยแอนติบอดีสำเร็จรูป คาดว่าจะแล้วเสร็จภายใน 2 สัปดาห์ เพื่อให้ทันต่อการระบาดใหญ่ของบรรดาสายพันธุ์ย่อยในกลุ่ม XBB ที่กำลังเกิดขึ้น
ศูนย์จีโนมฯ รพ. รามาธิบดี ยังได้ทำการวิเคราะห์จากรหัสพันธุกรรมทั้งจีโนมพบว่าโอไมครอนลูกผสม XBB.1.16 มีความได้เปรียบในการเติบโต-แพร่ระบาด (relative growth advantage) เหนือกว่า
XBB.1.5 ประมาณ 84%
BN.1.3 ประมาณ 138%
BN.1.2 ประมาณ 135%
XBB.1.9.1 ประมาณ 55%
XBB.1.9.2 ประมาณ 48%
คาดว่า XBB.1.16 จะเข้ามาแทนที่ BN1.3, BN.1.2, และ XBB.1.5 ในประเทศไทยภายใน 1-3 เดือนจากนี้
ผู้เชี่ยวชาญทั่วโลกพบว่า XBB.1.16 มีค่าระดับการติดเชื้อยังผล (Effective reproduction number)สูงกว่า XBB.1 และ XBB.1.5 ประมาณ 1.27 และ 1.17 เท่า ตามลำดับ ซึ่งบ่งชี้ว่า XBB.1.16 มีแนวโน้มที่จะแพร่กระจายไปทั่วโลกโดยเข้ามาแทนที่สายพันธุ์หลักที่ระบาดอยู่ในขณะนี้คือ XBB.1 และ XBB.1.15
หมายเหตุ
ค่าระดับการติดเชื้อยังผล (Re): เป็นพารามิเตอร์ทางระบาดวิทยาที่สำคัญซึ่งวัดความสามารถในการแพร่เชื้อของโรคติดเชื้อ
แสดงถึง: จำนวนผู้ติดเชื้อรายใหม่โดยเฉลี่ยที่เกิดจากผู้ติดเชื้อรายเดียว
Re > 1: การระบาดใหญ่ขึ้น (ผู้ติดเชื้อแต่ละคนแพร่เชื้อไปยังบุคคลอื่นมากกว่าหนึ่งคน)
Re < 1: การระบาดลดลง (ผู้ติดเชื้อแต่ละคนติดเชื้อน้อยกว่าหนึ่งคน)
Re = 1: สถานการณ์คงที่ (จำนวนผู้ติดเชื้อคงที่)
การรักษาการติดเชื้อโอไมครอนลูกผสมกลุ่ม XBB* อันรวมถึง XBB.1.16 ด้วยแอนติบอดีสำเร็จรูป
ในกลุ่มเปราะบางที่ติดเชื้อโควิดในบางกรณีแพทย์อาจให้ยาแอนติบอดีสำเร็จรูป (monoclonal antibody) เพื่อให้ร่างกายมีภูมิคุ้มกันในทันที เพื่อต่อสู้กับเชื้อโควิดในร่างกาย อาทิ
แบมลานิวิแมบ (Bamlanivimab/LY-CoV555) มีเป้าหมายเข้าจับกับโปรตีนหนามของ ไวรัสโควิด-19 ซึ่งช่วยป้องกันไม่ให้ไวรัสเข้าสู่เซลล์
อีเทเสวิแมบ (Etesevimab/LY-CoV016) มักใช้ร่วมกับ แบมลานิวิแมบ เพื่อประสิทธิภาพที่ดีขึ้น
คาซิริวิแมบ (Casirivimab/REGN10933 และ อิมเดวิแมบ (Imdevimab/REGN10987) มีเป้าหมายที่โปรตีนหนามของไวรัสโควิด -19 เมื่อใช้ร่วมกันในรูปยาผสมจะเรียกว่า โรนาพรีเว่ (Ronapreve หรือ REGEN-COV สามารถลดความเสี่ยงของโควิด-19 รุนแรงได้
โซโทรวิแมบ (Sotrovimab/VIR-7831) เป็นโมโนโคลนอลแอนติบอดีชนิดเดียวในปัจจุบันที่สามารถจับกับส่วนหนามและทำลายโอไมครอนสายพันธุ์ย่อย XBB.1, XBB.1.5, และ XBB.1.16 ลงได้ ลดความเสี่ยงที่จะเจ็บป่วยต้องพักรักษาตัวในโรงพยาบาลหรือลดอัตราการเสียชีวิตในผู้ป่วยติดเชื้อโควิด-19 โดยเฉพาะกลุ่มโอไมครอน XBBสถาบันสาธารณสุข โรเบิร์ต ค็อค (Robert Koch Institute/RKI) ประเทศเยอรมัน แนะนำให้ใช้ยาต้านไวรัส แพกซ์โลวิด, เรมเดซิเวียร์ (Paxlovid, Remdesivir) และ แอนติบอดีสำเร็จรูป โซโทรวิแมบ (Sotrovimab) ในการรักษาผู้ติดเชื้อโควิด-19
โทซิลิซูแมบ (Tocilizumab) จากการวิจัยพบว่าสามารถใช้รักษาผู้ป่วยที่มีอาการรุนแรงของโควิด-19 ได้ ซึ่งเข้าระงับการตอบสนองทางภูมิคุ้มกันที่มากเกินไปหรือที่เรียกว่า "พายุไซโตไคน์" อันนำไปสู่การอักเสบรุนแรง อาการหายใจลำบากเฉียบพลัน (ARDS)
ซิลกาวิแมบ และ ทิซาจวิแมบ (Cilgavimab & Tixagevimab) - โมโนโคลนอลแอนติบอดีเหล่านี้มีเป้าหมายที่ส่วนต่าง ๆ ของโปรตีนของไวรัสโควิด-19 เมื่อใช้ร่วมกันเรียกว่า อีวูเชลด์ (Evusheld/AZD7442) เป็นยาแอนติบอดีออกฤทธิ์ยาว (Long-acting Antibody - LAAB) ซึ่งได้รับการพัฒนาเพื่อป้องกันการติดเชื้อโควิด-19
การรักษาการติดเชื้อโอไมครอนลูกผสมกลุ่ม XBB* อันรวมถึง XBB.1.16 ด้วยยาต้านไวรัส จากข้อมูลล่าสุดพบว่ายาต้านไวรัส เรมเดซิเวียร์ (ให้ทางเส้นเลือดดำ), มอลนูพิราเวียร์, แพกซ์โลวิด, และเอนซิเทรลเวียร์ (remdesivir, molnupiravir, Paxlovid, and ensitrelvir) ซึ่งใช้รับประทานยังคงสามารถยับยั้งการเพิ่มจำนวนของ XBB, XBB.1.5 และน่าจะรวมถึง XBB.1.16 ได้เป็นอย่างดี ยังไม่พบเชื้อโควิด-19 ดื้อยา
การป้องกันด้วยวัคซีน
ทีมวิจัยจากประเทศญี่ปุ่นได้แสดงให้เห็นว่า XBB.1.16 สามารถหลบเลี่ยงภูมิคุ้มกันที่ผู้ติดเชื้อได้รับจากการติดเชื้อโอไมครอน BA.2 มาก่อนประมาณ 18 เท่าเมื่อเทียบกับสายพันธุ์ดั้งเดิม (B.1.1) ในขณะที่ XBB.1.16 หลบเลี่ยงภูมิคุ้มกันที่ผู้ติดเชื้อได้รับจากการติดเชื้อโอไมครอนBA.5 มาก่อนประมาณ 37 เท่าเมื่อเทียบกับสายพันธุ์ดั้งเดิม (B.1.1) แสดงให้เห็นว่าภูมิคุ้มกันที่เราได้มาจากการฉีดวัคซีนรุ่นแรกและวัคซีนเข็มกระตุ้นชนิดสองสายพันธุ์ (bivalent covid-19 booster) หรือภูมิคุ้มกันผู้ที่เคยติดเชื้อโอไมครอน BA.2 หรือ BA.4/BA.5 มาก่อนอาจไม่ช่วยป้องกันการติดเชื้อโอไมครอน XBB.1, XBB.1.5, และ XBB.1.16 ได้ดีนัก แต่จะช่วยป้องกันการเจ็บป่วยรุนแรงหรือการเสียชีวิตจากปอดอักเสบได้ดีไม่แตกต่างจากโอไมครอนสายพันธุ์อื่นๆ อย่างมีนัยสำคัญ
เหตุที่หลายฝ่ายคาดว่าโอไมครอน XBB.1.16 จะมาแทนที่ทุกสายพันธุ์ที่ระบาดอยู่ในปัจจุบันอาจเนื่องมาจาก (1) มีการกลายพันธุ์โดยเฉพาะส่วนหนามแตกต่างจากโอไมครอน XBB.1.5 และ/หรือ (2) มีกลายพันธุ์เปลี่ยนแปลงโครงสร้างโปรตีนส่วนอื่นที่ไม่ใช่ส่วนหนามร่วมด้วยอันอาจมีส่วนช่วยเพิ่มประสิทธิภาพการเติบโต-แพร่ระบาด (relative growth advantage) ของไวรัส
ดร. อริจิตต์ จักรวารตี (Arijit Chakravarty) จากสถาบัน Fractal Therapeutics ในเมืองเล็กซิงตัน รัฐแมสซาชูเซตส์ สหรัฐอเมริกา ร่วมมือกับนักวิจัยจากสถาบันต่างๆ ศึกษาข้อจำกัดของการพึ่งพาวัคซีนเพียงอย่างเดียวในการควบคุมและหยุดยั้งการกลายพันธุ์ของไวรัสโควิด-19 พวกเขาสรุปว่าอัตราการแพร่เชื้อที่สูงยังคงสามารถนำไปสู่การกลายพันธุ์เกิดสายพันธุ์ใหม่ได้ แม้ว่าจะมีการฉีดวัคซีนอย่างแพร่หลาย โดยเน้นย้ำถึงความจำเป็นที่ต้องนำการวัคซีนเข้าผนวกกับมาตรการอื่น เช่น กินร้อน ช้อนกลาง ใส่หน้ากากอนามัย เว้นระยะห่างทางสังคม การใช้ยาต้านไวรัส และแอนติบอดีสังเคราะห์ ฯลฯ เพื่อลดการแพร่ระบาดของโควิด-19
....
#โอไมครอน
#ศูนย์จีโนมทางการแพทย์
Center for Medical Genomics
 ข่าวทั้งหมด
ข่าวทั้งหมด